Kedves hetedikesek!
Ez a sok szöveg azért van itt, mert lényeges és egy részét kifelejtették a tankönyvből.
Ezeket légy szíves gyöngyírással belehelyezni a füzetedbe, csak utána jöhet a könyv.
Természetesen el is magyarázom!
A kémiai kötések
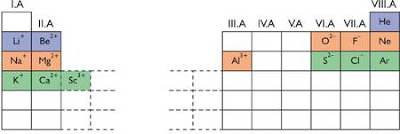
Az elemek azonos (protonszámú) atomokból épülnek fel.
A nemesgázok (VIII. A főcsoport) mindig atomokból állnak, mert stabil az elektronszerkezetük. A stabil elektronszerkezet azt jelenti, hogy 2 (He) vagy 8 vegyértékelektronjuk van(Ne, Ar, Kr, Xe , Rn).
Az összes többi atom arra törekszik, hogy valahogyan elérje a stabil elektronszerkezetet, vagyis 2 vagy 8 vegyértékelektronja legyen.
Ennek érdekében az atomok között valamilyen kapcsolat, átalakulás jön létre. Ennek a kapcsolatnak a neve a kémiai kötés.
1.Mi akémiai kötés?
A kémiai részecskék (atomok, ionok, molekulák) között létesülő kapcsolatot kémiai kötésnek nevezzük.
A kötések közötti erősség szerint:
Elsőrendű (erős)kötések: ionos, kovalens, fémes kötés (ezekről tanulunk)
Másodrendű(gyöngébb) kötés: pl.:molekulák közötti kapcsolat
A fémekre a fémes kötés jellemző.
Elemmolekulák
A szobahőmérsékleten GÁZ-halmazállapotú elemek (a nemesgázok kivételével) kétatomos molekulákból állnak. Ezek a hidrogén H2, az oxigén O2, a nitrogén N2, és a klór Cl2
A két atomot közös elektronpár(ok) tartják össze. Az atomok között kovalens kötés jön létre.
2.Mi a kovalens kötés?
Az atomok között közös elektronpárral létrejött kapcsolatot kovalens kötésnek nevezzük.
3. Mit nevezünk molekulának?
A molekulák olyan semleges kémiai részecskék, amelyekben meghatározott számú atom kapcsolódik össze kovalens kötéssel.
A molekulákat képlettel jelöljük.
Eddig írd le!😓
Ez így nincs a könyvben, ezt a füzetből tanuld meg. Utána a könyv 83-84. oldalát legalább kétszer olvasd el! (Csak a hidrogén kell egyelőre)
Videón nézd meg, milyen kísérlettel lehet előállítani hidrogéngázt!
Az elemek jellemzése rajta van a beragasztott lapon is, nem kell külön leírni!
Hidrogéngáz, hidrogénmolekula H2
- színtelen, szagtalan gáz
- levegőnél kisebb (a legkisebb) sűrűségű gáz
- vízben nem oldódik
- éghető, vízzé ég el (H2 + O2 → H2O )
- levegővel (oxigénnel) keveredve robban (DURRANÓGÁZ)
Előállítása: vízbontással
cinkre sósavat csepegtetünk
A hidrogéngáz hidrogénmolekulákból áll,
amelyben két hidrogénatom kapcsolódik kovalens kötéssel.
A hidrogéngáz és hidrogénmolekula képlete is H2Ismét nézd meg a videót!
Hidrogén előállítása, durranogázpróba: https://www.youtube.com/watch?v=Gh_xv8oWwpsKövetkező elemünk a klór, a szagával mindenki találkozott az uszodában,
lehet, hogy a fürdőruháját is kifakította már.
A klór és a klórmolekula Cl2
- sárgászöld, szúrós szagú gáz
- levegőnél nagyobb sűrűségű
- köhögésre ingerlő, MÉRGEZŐ gáz (I.világháború)
- vízben oldódik, vizes oldata fertőtlenít (kórházak, uszodák)
- színtelenítő, fehérítő hatású
Előállítása: kálium-permanganátra sósavat csepegtetünk.
A klórmolekulában 2 klóratom kapcsolódik kovalens kötéssel.
A klórgáz klórmolekulákból áll.
A klórgáz és a klórmolekula jele: Cl2Nézz meg egy videót!
Klór előállítása, színtelenítő, fehérítő hatása: https://www.youtube.com/watch?v=JHVWD9Vi16AAz oxigént mindenki ismeri és egyfolytában találkozik vele!
Az oxigén és molekuláinak jele: O2
- színtelen, szagtalan
- levegőnél kicsit nagyobb sűrűségű gáz
- nem ég, az égést táplálja
- élethez nélkülözhetetlen
- vízben rosszul oldódik (KELL, hogy oldódjon!!)
Előállítása: vízbontással
kálium-permanganát hevítésével
Az oxigéngáz oxigénmolekulákból áll, amelyekben két oxigénatom
kapcsolódik össze kovalens kötéssel.
Az oxigéngáz és az oxigénmolekula jele: O2Nézz meg egy videót, remélem mindenkinek ismerős a kísérlet!
Oxigén előállítása, kimutatása: https://www.youtube.com/watch?v=UD4M2Xjt39YAz utolsó elemi gázunk, amely kétatomos molekulákból a nitrogén.
A nitrogéngáz, a nitrogénmolekula N2
- színtelen, szagtalan gáz
- a levegő 78%-a
- az égést nem táplálja
- közömbös, kis reakcióképességű gáz
- vízben nem oldódik
Előállítása cseppfolyós levegőből.
A nitrogéngáz nitrogénmolekulákból áll,
a nitrogénmolekulában két nitrogénatom kapcsolódik kovalens kötéssel.
A nitrogéngáz és a nitrogénmolekula jele: N2
Még egy videó a FOLYÉKONY nitrogénről (JÓ):